Extraido de la wikipedia ([URL]http://es.wikipedia.org/wiki/Pila_de_combustible_alcalina[/URL]) :
La pila de combustible alcalina (AFC, o Alcaline Fuel Cell en su denominación anglosajona), es una de las más desarrolladas tecnologías dentro de las [URL="http://foros.monografias.com/wiki/Pila_de_combustible"]
pilas de combustible[/URL]
, y es el tipo de pila de combustible que llevó al hombre a la [URL="http://foros.monografias.com/wiki/Luna"]
Luna[/URL]
. La AFC consume [URL="http://foros.monografias.com/wiki/Hidr%C3%B3geno"]
hidrógeno[/URL]
y [URL="http://foros.monografias.com/wiki/Ox%C3%ADgeno"]
oxígeno[/URL]
, produciendo [URL="http://foros.monografias.com/wiki/Agua"]
agua[/URL]
, [URL="http://foros.monografias.com/wiki/Calor"]
calor[/URL]
y [URL="http://foros.monografias.com/wiki/Electricidad"]
electricidad[/URL]
. Su efectividad es de las más elevadas en este tipo de tecnologías, llegando a alcanzar un rendimiento del 70%.
Esta pila produce la energía a través de una [URL="http://foros.monografias.com/wiki/Reacci%C3%B3n_redox"]
reacción redox[/URL]
entre el hidrógeno y el oxígeno. En el ánodo, el hidrógeno es [URL="http://foros.monografias.com/wiki/Oxidaci%C3%B3n"]
oxidado[/URL]
según la reacción:

 produciendo agua y soltando 2
produciendo agua y soltando 2 [URL="http://foros.monografias.com/wiki/Electr%C3%B3n"]
electrones[/URL]
. Los electrones fluyen a través de un circuito externo y regresan al cátodo, [URL="http://foros.monografias.com/wiki/Reducci%C3%B3n"]
reduciendo[/URL]
al oxígeno según la reacción:

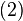 produciendo iones hidróxidos. La reacción global consume una molécula de Oxígeno y 2 de Hidrógeno para producir 2
produciendo iones hidróxidos. La reacción global consume una molécula de Oxígeno y 2 de Hidrógeno para producir 2 [URL="http://foros.monografias.com/wiki/Mol%C3%A9cula"]
moléculas[/URL]
de agua. La electricidad y el calor son subproductos de esta reacción
entonces ¿donde van los electrones generados si no salen porque no se mueven de sus átomos?
Un saludo








Marcadores